Cтраница 4
Атомы углерода способны соединяться друг с другом, образуя более сложные молекулы, но в отличие от Н2, С2 или Na, которые насыщены и слабо притягиваются друг к другу, а потому при обычных условиях газообразны, молекулы углерода не насыщены и чрезвычайно склонны к конденсации в твердое состояние; они остаются газообразными лишь при очень высоких температурах.
То обстоятельство, что здесь, как и во всех реакциях, во взаимодействие вступают молекулы, не при-нято в расчет; если же принять во внимание, что молекула представляет соединение однородных атомов, что, может быть, даже молекула углерода состоит из многих углеродных атомов, на что, невидимому, указывает ее постоянство, то оправдывается допущение, что отделению этих углерод - ных атомов друг от друга, предшествующему их соединению с кислородом, соответствует термический эффект - по всей вероятности, поглощение тепла, тогда как при горении окиси углерода в реакции принимает участие отдельный атом углерода. Точно так же образование воды указывает на два (а может быть и на три, если принять молекулу кислорода 02) момента: разделение атомов водорода, ранее связанных в молекулы, и соединение их с кислородом. Каждому из этих моментов должен соответствовать термический эффект.
По полученным данным нельзя сделать однозначный вывод о составе пара углерода над карбидами, однако тот факт, что при расчете реакции (18) на Сз получаем для аш значение больше 1, говорит в пользу того, что над карбидами в области исследуемых температур преобладают атомы, а не молекулы углерода.
В Берклеевской национальной лаборатории (США) создана новая форма твердого углерода Сзб - Его молекула состоит из 36 атомов углерода. Молекулы углерода С36 возникают вместе с фуллеренами С60 в пламени дугового разряда между двумя графитовыми электродами. Исследователи полагают, что молекулы С3 & могут обладать интересными электрическими и химическими свойствами.
Спектрами лунных извержений, вероятно, заинтересуются астробиологи. Ведь молекулы углерода, азота, во - дорода, выходящие из лунных кратеров, дают основание полагать, что в недрах нашего спутника немало органических соединений.
Будет ли устойчива молекула углерода состава Сг. Какую кристаллическую решетку образуют атомы углерода в алмазе и графите.
Это объясняется полимерным строением молекул углерода, поэтому и графит, и алмаз, состоящие из одинаковых, только углеродных атомов, относят к полимерам. Любой кристалл алмаза представляет собой, по существу, идеально построенный трехмерный полимер. В графите полимерная упорядоченность распространяется только по плоскости. Существуют и одномерные (линейные) полимеры углерода: карбин и поликумулен. В настоящее время понятие фуллерены применяется к широкому классу многоатомных молекул углерода Сп (п от 24 и более) и твердым телам на их основе. Однако еще несколько лет назад фуллереном (точнее бакминстерфуллереном) называли молекулу Сео, атомы которой располагаются на поверхности сферы в вершинах 12 равносторонних пятиугольников и 20 равносторонних шестиугольников. Ее радиус составляет 0 357 нм. Уникальные свойства фуллеренов привлекают внимание ученых всего мира.
Повышение светимости факела объясняется тем, что при нагреве углеводородных газов происходит их распад на более простые соединения - атомарный углерод и водород. В связи с недостатком кислорода молекулы углерода образуют мельчайшие частицы твердого углерода (сажи), которые, раскаляясь, придают пламени светимость.
Сольватация рассматривается на молекулярном уровне и включает всю совокупность взаимодействий, осуществляющихся в растворе, которые в зависимости от свойств растворителя и растворенного вещества могут иметь различную природу и проявляться по-разному. Например, сольватация молекул иода молекулами четы-реххлористого углерода, молекул фосфора или серы молекулами сероуглерода осуществляется исключительно за счет слабого ван-дерваальсова взаимодействия, но все же энергия сольватации оказывается больше, чем энергия взаимодействия частиц в молекулярных кристаллах растворяющихся веществ. Как правило, из таких молекулярных растворов растворитель легко удаляется, а растворенное вещество остается в химически неизменном виде. При испарении растворителей из перечисленных растворов можно получить хорошо образованные кристаллы иода, фосфора, серы.
Cтраница 2
В последнее время появилось упоминание о патенте Карабачека (1931 г.), согласно которому алмазы образуются при кристаллизации углерода из расплава; в состав последнего входит железо и доменный шлак, углерод, а также твердая углекислота и жидкая окись углерода.
Реагирующее углеводородное сырье при контакте с поверхностью катализатора разлагается на углерод п водород с последующим образованием небольших кристаллов карбида железа РезСз, которые образуются при эннтаксналыюп кристаллизации углерода. Полученные небольшие кристаллы РегСз равномерно распределены по каталитически активной поверхности металла. На определенной стадии развития небольшие кристаллы РезСз уносятся углеродом с металлической подложки.
Наиболее типичными атомными кристаллами являются кристаллы алмаза. При кристаллизации углерода его атомы находятся в состоянии s p3 и орбитали их полностью гибридизированы. Координационное число кристалла алмаза 4, что также соответствует правилу Юм-Розери. Кристаллическая решетка алмаза представляет собой центрированный тетраэдр, который можно отнести к кубической системе, так как он вписывается в куб, а макроформа кристаллов алмаза представляет собой модифицированный куб.
Сопоставление теплот сгорания алмаза (394 1 кдж / г-ат) графита (396 3 / сдэк / г-ат) и карбина (356 1 кдж / г-ат) говорит о том, что графит - наиболее стабильная модификация углерода. Поэтому при кристаллизации углерода, например из металлических растворов, образуется графит, а при сильном нагревании до 1000 - 1500 С (без доступа воздуха) алмаз превращается в графит. Перевод же графита в алмаз возможен лишь при очень высоких давлениях и температурах (см. стр. При нагревании до 2800 С карбин также превращается в графит.
Муассана, получил при кристаллизации углерода в расплавленном серебре прозрачные и темные кристаллики. Они царапали самый твердый после алмаза минерал - корунд и сгорали, образуя углекислый газ.
Существует предположение, что исходным материалом для природного синтеза-алмазов служил углерод, возникавший в результате восстановления (при высоких температурах и под большим давлением) карбонатных пород двухвалентным железом по примерной суммарной схеме: СаС03 5FeO Са (РеО2) г Fe3O4 С. Необходи - мое для кристаллизации углерода в форме алмаза очень высокое давление (рис. Х-1) создавалось за счет его случайных местных повышений.
Теплота сгорания графита на 0 20 ккал / г-атом ниже, чем теплота сгорания алмаза, откуда следует, что графит является более стабильной модификацией углерода. Поэтому в условиях, при которых возможна кристаллизация углерода, нормальным является образование графита. Так, растворенный в жидком железе углерод при охлаждении частично-выделяется в виде графита. Этим и объясняется серая окраска чугуна.
Теплота сгорания графита на 0 20 ккал / г-атом ниже, чем теплота сгорания алмаза, откуда следует, что графит является более стабильной модификацией углерода. Поэтому в условиях, при которых возможна кристаллизация углерода, нормальным является образование графита. Так, растворенный в жидком железе углерод при охлаждении частично выделяется в виде графита. Этим и объясняется серая окраска чугуна.
Получение именно этих двух карбидов: карбида кальция и карбида кремния, обратилось в мощные отрасли химической промышленности. Так же, как Муассан для той же целилпредпринял кристаллизацию углерода из железа, воспроизводя условия образования алмазов в железных метеоритах, была сделана попытка воспроизвести в лабораторных условиях образование алмазов в неметаллических горных породах. Широкая распространенность в природе известняков побудила сплавить уголь именно с известняком. Таким образом вместо ал-v lytasa и был получен карбид кальция - источник ацетилена, газообразного горючего, превосходящего по развиваемой им температуре все другие обычные горючие газы, а потому особенно пригодного для сварки и резки металла.
Она сводится к тому, что по мере увеличения химического возраста горючая масса все больше освобождается ог наиболее непрочных содержащих кислород компонентов и обогащается углеродом. В этом смысле антрацит такой отощенности является предельным топливом, в угольном веществе которого стадии химических преобразований практически уже завершились и заметно развились стадии преобразований физических (кристаллизация углерода), делающих его в значительной мере химически инертным.
Рост углеродного волокна контролируется, с одной стороны, кинетическими факторами реакции каталитического дегидрирования углеводородного сырья. С другой стороны, па рост углеродного волокна накладывается жесткое кристаллографическое ограничение неизменности диаметра волокна, приводящее к остановке его роста при изменении условий реакции, и наличие баланса неизменности скоростей образования и кристаллизации углерода на единичном фрагменте катализатора.
Рост углеродного волокна контролируется, с одной стороны, кинетическими факторами реакции каталитического дегидрирования углеводородного сырья. С другой стороны, на рост углеродного волокна накладывается жесткое кристаллографическое ограничение неизменности диаметра волокна, приводящего к остановке его роста при изменении условий реакции, и наличие баланса неизменности скоростей образования и кристаллизации углерода на единичном фрагменте катализатора.
При этом неизменно получали не алмаз, а графит. Внимание было обращено также на возможность получения алмаза при кристаллизации углерода в результате разложения органических и неорганических углеродсодержащих соединений.
Cтраница 1
Плавление углерода, кремния, галлия, германия, мышьяка, сурьмы, теллура, висмута связано с большими изменениями их строения и свойств. Описание этих изменений имеется в гл.
Определены условия плавления углерода : при давлениях выше 60 ГПа предполагается существование металлического углерода. На рис. 1 представлен современный вид Р - Г - диаграммы фазовых равновесий углерода. Линия равновесия Г 2 А описывается уравнением Р 7000 27Г, где Р - давление, атм; Т - абсолютная температура, К.
Особые трудности вызывает определение температуры плавления углерода, у которого вследствие значительного давления пара точка плавления сильно зависит от продукта, получающегося после нагревания.
Строение жидкого углерода пока еще не изучено. Предполагается, что плавление углерода сопровождается ростом среднего координационного числа, причем жидкий углерод - металл.
Известно, что благодаря слоистой структуре графит обладает ценными смазывающими свойствами. Очень высокая температура плавления углерода способствует все большему использованию его в качестве конструкционного материала в высокотемпературных технологических процессах. Благодаря некоторым физическим свойствам графит получил широкое применение в ядерных реакторах.
Отвод тепла от эмиттирующей поверхности может осуществляться теплопроводностью, излучением и испарением вещества катода. Рассмотрим предельные оценки указанных факторов, исходя из теоретической температуры плавления углерода - 5000 К и высоты микровыступа 200 А.
Какие-либо экспериментальные данные по теплоте плавления графита отсутствуют. Значения теплоты плавления 11 и 10 ккал / г-атом, вычисленные соответственно Рышкевичем и Фаянсом по разности наклона кривых давления паров твердого и жидкого углерода, недостоверны. Оценка величины энтропии и теплоты плавления углерода может быть сделана на основании величин энтропии плавления элементов IV (основной) группы Периодической системы.
Плавление неметаллов с координационном решеткой сопровождается разрывом ковалентной связи, увеличением координационного числа атомов и возрастанием межъядерных расстояний. Предполагают, что таким же изменением координационного числа атомов сопровождается плавление углерода и кремния.
Обсудим, как изменяется температура плавления в ряду С - Si - Ge - Sn - Pb. Плавление неметаллов сопровождается разрывом ковалентной связи, увеличением координационного числа атомов и возрастанием межъядерных расстояний. Предполагают, что таким же изменением координационного числа атомов сопровождается плавление углерода и кремния.
Углерод является одним из наиболее замечательных элементов. Это утверждение основано прежде всего на практически неисчерпаемом многообразии органических соединений. Указанное обстоятельство предопределяет, в свою очередь, огромное разнообразие структуры и свойств (в том числе электрохимических и электрокаталитических) углеродных материалов. Это обусловлено двумя основными факторами. Во-первых, углеродные материалы легко образуются из разнообразных природных и синтетических соединений углерода путем их пиролиза. Во-вторых, чрезвычайно высокое значение температур испарения и плавления углерода предопределяет хорошую стабильность углеродных материалов даже в жестких условиях. Характеристики углеродных материалов, которые правильнее всего рассматривать как сложные полимерные структуры, определяются не индивидуальными свойствами углерода, а исходных углеродсодержащих веществ и условиями их обработки.
Страницы: 1
ФУЛЛЕРЕНЫ – НОВАЯ АЛЛОТРОПНАЯ ФОРМА УГЛЕРОДА
1. ТЕОРЕТИЧЕСКИЙ РАЗДЕЛ
1.1. Известные аллотропные формы углерода
До недавнего времени было известно, что углерод образует три аллотропных формы: – алмаз, графит и карбин. Аллотропия, от греч. Allos - иной, tropos - поворот, свойство, существование одного и того же элемента в виде различных по свойствам и строению структур В настоящее время известна четвертая аллотропная форма углерода, так называемый фуллерен (многоатомные молекулы углерода С n).
Происхождение термина "фуллерен" связано с именем американского архитектора Ричарда Букминстера Фуллера, конструировавшего полусферические архитектурные конструкции, состоящие в виде шестиугольников и пятиугольников.
В середине 60-х годов Дэвид Джонс конструировал замкнутые сфероидальные клетки из своеобразным образом свернутых графитовых слоев. Было показано, что в качестве дефекта, внедренного в гексагональную решетку обычного графита, и приводящего к образованию сложной искривленной поверхности, может быть пятиугольник.
В начале 70-х годов физхимик–органик Е.Осава предположил существование полой, высокосимметричной молекулыС 60 , со структурой в виде усеченного икосаэдра, похожей на футбольный мяч. Чуть позже (1973 г.) российские ученые Д.А. Бочвар и Е.Г. Гальперин сделали первые теоретические квантово-химические расчеты такой молекулы и доказали ее стабильность.
В 1985 году, коллективу ученых: Г.Крото (Англия, Сассекский университет), Хит, 0"Брайен, Р.Ф.Керл и Р. Смолли (США, Университет Раиса) удалось обнаружить молекулу фуллерена при исследовании масс-спектров паров графита после лазерного облучения твердого образца.
Первый способ получения и выделения твердого кристаллического фуллерена был предложен в 1990 г. В.Кречмером и Д.Хафманом с коллегами в институте ядерной физики в г. Гейдельберге (Германия).
В 1991 году японский ученый Иджима на полярном ионном микроскопе впервые наблюдал различные структуры, составленные, как и в случае графита, из шестичленных колец углерода: нанотрубки, конусы, наночастицы.
В 1992 в природном углеродном минерале – шунгите (свое название этот минерал получил от названия поселка Шуньга в Карелии) были обнаружены природные фуллерены.
В 1997 году Р.Е.Смолли, Р.Ф.Керл,Г.Крото получили Нобелевскую премию по химии за изучение молекул С 60 , имеющих фору усеченного икосаэдра.
Рассмотрим структуру аллотропных форм углерода: алмаза, графита и карбина.
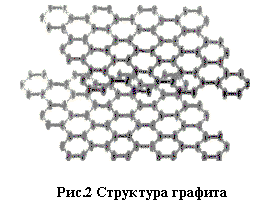 |
|||
Алмаз - Каждый атом углерода в структуре алмаза расположен в центре тетраэдра, вершинами которого служат четыре ближайших атома. Соседние атомы связаны между собой ковалентными связями (sp 3 -гибридизация). Такая структура определяет свойства алмаза как самого твердого вещества, известного на Земле.
Графит находит широкое применение в самых разнообразных сферах человеческой деятельности, от изготовления карандашных грифелей до блоков замедления нейтронов в ядерных реакторах. Атомы углерода в кристаллической структуре графита связаны между собой прочными ковалентными связями (sp 2 - гибридизация) и формируют шестиугольные кольца, образующие, в свою очередь, прочную и стабильную сетку, похожую на пчелиные соты. Сетки располагаются друг над другом слоями. Расстояние между атомами, расположенными в вершинах правильных шестиугольников, равно 0,142 нм., между слоями – 0,335 нм. Слои слабо связаны между собой. Такая структура - прочные слои углерода, слабо связанные между собой, определяет специфические свойства графита: низкую твёрдость и способность легко расслаиваться на мельчайшие чешуйки.
Карбин конденсируется в виде белого углеродного осадка на поверхности при облучении пирографита лазерным пучком света. Кристаллическая форма карбина состоит из параллельно ориентированных цепочек углеродных атомов с sp-гибридизацией валентных электронов в виде прямолинейных макромолекул полиинового (-С= С-С= С-...) или кумуленового (=С=С=С=...) типов.
Известны и другие формы углерода, такие как аморфный углерод, белый углерод (чаоит) и т.д. Но все эти формы являются композитами, то есть смесью малых фрагментов графита и алмаза.
1.2.Геометрия молекулы фуллерена и кристаллическая решетка фуллерита
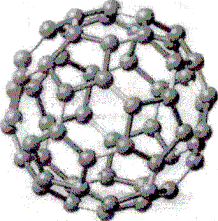
Рис.3 Молекула фуллерена С 6 0
В противоположность алмазу, графиту и карбину, фуллерен является новой формой углерода по существу. Молекула С 60 содержит фрагменты с пятикратной симметрией (пентагоны), которые запрещены природой для неорганических соединений. Поэтому следует признать, что молекула фуллерена является органической молекулой, а кристалл, образованный такими молекулами (фуллерит ) – это молекулярный кристалл, являющийся связующим звеном между органическим и неорганическим веществом.
Из правильных шестиугольников легко выкладывается плоская поверхность, однако ими не может быть сформирована замкнутая поверхность. Для этого необходимо часть шестиугольных колец разрезать и из разрезанных частей сформировать пятиугольники. В фуллерене плоская сетка шестиугольников (графитовая сетка) свернута и сшита в замкнутую сферу. При этом часть шестиугольников преобразуется в пятиугольники. Образуется структура – усеченный икосаэдр, который имеет 10 осей симметрии третьего порядка, б осей симметрии пятого порядка. Каждая вершина этой фигуры имеет трех ближайших соседей. Каждый шестиугольник граничит с тремя шестиугольниками и тремя пятиугольниками, а каждый пятиугольник граничит только с шестиугольниками.Каждый атом углерода в молекуле C 60 находится в вершинах двух шестиугольников и одного пятиугольника и принципиально неотличим от других атомов углерода. Атомы углерода,образующие сферу, связаны между собой сильной ковалентной связью. Толщина сферической оболочки 0,1 нм, радиус молекулы С 60 0,357 нм. Длина связи С-С в пятиугольнике - 0,143 нм, в шестиугольнике – 0,139 нм.
Молекулы высших фуллеренов С 70 С 74 , С 76 , С 84 , С 164 , С 192 , С 216 , также имеют форму замкнутой поверхности.
Фуллерены с n< 60 оказались неустойчивыми, оказались неустойчивыми, хотя из чисто топологических соображений наименьшим возможным фуллереном является правильный додекаэдр С 20 .
Кристаллический фуллерен, который был назван фуллеритом имеет гранецентрированную кубическую решетку (ГЦК), пространственная группа (Fm3m).. Параметр кубической решетки а 0 = 1.42 нм, расстояние между ближайшими соседями – 1 нм. Число ближайших соседей в ГЦК решетке фуллерита –12.
Между молекулами С 60 в кристалле фуллерита существует слабая связь Ван-дер-Ваальса. Методом ядерного магнитного резонанса было доказано, что при комнатной температуре молекулы С 60 , вращаются вокруг положения равновесия с частотой 10 12 1/с. При понижении температуры вращение замедляется. При 249К в фуллерите наблюдается фазовый переход первого рода, при котором ГЦК решетка (пр. гр.Fm3m) переходит в простую кубическую (пр.гр. РаЗ). При этом объем фулдерита увеличивается на 1%. Кристалл фуллерита имеет плотность 1,7 г/см 3 , что значительно меньше плотности графита (2,3 г/см 3) и алмаза (3,5 г/см).
Молекула С 60 сохраняет стабильность в инертной атмосфере аргона вплоть до температур порядка 1700 К. В присутствии кислорода при 500 К наблюдается значительное окисление с образованием СО и CO 2 . При комнатной температуре окисление происходит при облучении фотонами с энергией 0,55 эВ. что значительно ниже энергии фотонов видимого света (1,54 эВ). Поэтому чистый фуллерит необходимо хранить в темноте. Процесс, продолжающийся несколько часов, приводит к разрушению ГЦК- решетки фуллерита и образованию неупорядоченной структуры, в которой на исходную молекулу Сбо приходится 12 атомов кислорода. При этом фуллерены полностью теряют свою форму.
1.3. Получение фуллеренов
Наиболее эффективный способ получения фуллеренов основан на термическом разложении графита. Используется как электролитический нагрев графитового электрода, так и лазерное облучение поверхности графита На рис. 4 показана схема установки для получения фуллеренов, которую использовал В.Кретчмер. Распыление графита осуществляется при пропускании через электроды тока с частотой 60 Гц, величина тока от 100 до 200 А, напряжение 10-20 В. Регулируя натяжение пружины, можно добиться, чтобы основная часть подводимой мощности выделялась в дуге, а не в графитовом стержне. Камера заполняется гелием, давление 100 Тор. Скорость испарения графита в этой установке может достигать 10г/В. При этом поверхность медного кожуха, охлаждаемого водой, покрывается продуктом испарения графита, т.е. графитовой сажей. Если получаемый порошок соскоблить и выдержать в течение нескольких часов в кипящем толуоле, то получается темно-бурая жидкость. При выпаривании ее во вращающемся испарителе получается мелкодисперсный порошок, вес его составляет не более 10% от веса исходной графитовой сажи., в нем содержится до 10% фуллеренов С 60 (90%) и С 70 (10%).Описанный дуговой метод получения фуллеренов получил название «фуллереновая дуга».
В описанном способе получения фуллеренов гелий играет роль буферного газа. Атомы гелия наиболее эффективно по сравнению с другими атомами «тушат» колебательные движения возбужденных углеродных фрагментов, препятствующих их объединению в стабильные структуры. Кроме того, атомы гелия уносят энергию, выделяющуюся при объединении углеродных фрагментов. Опыт показывает, что оптимальное давление гелия находится в диапазоне 100 Тор. При более высоких давлениях агрегация фрагментов углерода затруднена.

Рис.4. Схема установки для получения фуллеренов.
1 – графитовые электроды;
2 – охлаждаемая медная шина; 3 – медный кожух,
4 – пружины.
Изменение параметров процесса и конструкции установки ведет к изменению эффективности процесса и состава продукта. Качество продукта подтверждается как масс-спектрометрическими измерениями, так и другими методами (ядерный магнитный резонанс, электронный парамагнитный резонанс, ИК-спектроскопия и др.)
Обзор существующих в настоящее время способов получения фуллеренов и устройств установок, в которых получают для получения различные фуллеренов приведен в работе Г.Н.Чурилова.
Методы очистки и детектирования
Наиболее удобный и широко распространенный метод экстракциифуллеренов из продуктов термического разложения графита (термины: фуллерен-содержащей конденсат, фуллерено-содержащая сажа), а также последующей сепарации и очистки фуллеренов, основан на использовании растворителей и сорбентов.
Этот метод включает в себя несколько стадий. На первой стадии фуллерен-содержащая сажа обрабатывается с помощью неполярного растворителя, в качестве которого используются бензол, толуол и другие вещества. При этом фуллерены, обладающие значительной растворимостью в указанных растворителях, отделяются от нерастворимой фракции, содержание которой в фуллерен содержащей фазе составляет обычно 70-80 %. Типичное значение растворимости фуллеренов в растворах, используемых для их синтеза, составляет несколько десятых долей мольного процента. Выпаривание полученного таким образом раствора фуллеренов приводит к образованию черного поликристаллического порошка, представляющего собой смесь фуллеренов различного сорта. Типичный масс спектр подобного продукта показывает, что экстракт фуллеренов на 80 - 90 % состоит из С 60 и на 10 -15% из С 70 . Кроме того, имеется небольшое количество (на уровне долей процента) высших фуллеренов, выделение которых из экстракта представляет довольно сложную техническую задачу. Экстракт фуллеренов, растворенный в одном из растворителей, пропускается через сорбент, в качестве которого может быть использован алюминий, активированный уголь либо оксиды (Al 2 O 3 , SiO 2) с высокими сорбци- онными характеристиками. Фуллерены собираются этим металлом, а затем экстрагируются из него с помощью чистого растворителя. Эффективность экстракции определяется сочетанием сорбент-фуллерен-растворитель и обычно при использовании определенного сорбента и растворителя заметно зависит от типа фуллерена. Поэтому растворитель, пропущенный через сорбент с сорбированным в нем фуллереном, экстрагирует из сорбента поочередно фуллерены различного сорта, которые тем самым могут быть легко отделены друг от друга. Дальнейшее развитие описанной технологии получения сепарации и очистки фуллеренов, основанной на электродуговом синтезе фуллерено-содержащей сажи и её последующем разделении с помощью сорбентов и растворителей, привело к созданию установок, позволяющих синтезировать С 60 в количестве одного грамма в час.
1.4.Свойства фуллеренов
Кристаллические фуллерены и пленки представляют собой полупроводники с шириной запрещенной зоны 1,2-1,9 эВ и обладают фотопроводимостью. При облучении видимым светом электрическое сопротивление кристалла фуллерита уменьшается. Фотопроводимостью обладают не только чистый фуллерит, но и его различные смеси с другими веществами. Было обнаружено, что добавление атомов калия в пленки С 60 приводит к появлению сверхпроводимости при 19 К.
Молекулы фуллеренов, в которых атомы углерода связаны между собой как одинарными, так и двойными связями, являются трехмерными аналогами ароматических структур. Обладая высокой электроотрицательностью, они выступают в химических реакциях как сильные окислители. Присоединяя к себе радикалы различной химической природы, фуллерены способны образовывать широкий класс химических соединений, обладающих различными физико-химическими свойствами. Так, недавно получены пленки полифуллерена, в которых молекулы С 60 связаны между собой не ван-дер-ваальсовским, как в кристалле фуллерита, а химическим взаимодействием. Эти плёнки, обладающие пластическими свойствами, являются новьм типом полимерного материала. Интересные результаты достигнуты в направлении синтеза полимеров на основе фуллеренов. При этом фуллерен С 60 служит основой полимерной цепи, а связь между молекулами осуществляется с помощью бензольных колец. Такая структура получила образное название "нить жемчуга".
Присоединение к С 60 радикалов, содержащих металлы платиновой группы, позволяет получить ферромагнитные материалы на основе фуллерена. В настоящее время известно, что более трети элементов периодической таблицы могут быть помещены внутрь молекулы. С 60 . Имеются сообщения о внедрении атомов лантана, никеля, натрия, калия, рубидия, цезия, атомов редкоземельных элементов, таких как тербий, гадолиний и диспрозий.
Разнообразие физико-химических и структурных свойств соединений на основе фуллеренов позволяет говорить о химии фуллеренов как о новом перспективном направлении органической химии.
1.5. Применение фуллеренов
В настоящее время в научной литературе обсуждаются вопросы использования фуллеренов для создания фотоприемников и оптоэлектронных устройств, катализаторов роста,алмазных и алмазоподобных пленок, сверхпроводящих материалов, а также в качестве красителей для копировальных машин. Фуллерены применяются для синтеза металлов и сплавов с новыми свойствами.
Фуллерены планируют использовать в качестве основы для производства аккумуляторных батарей. Эти батареи, принцип действия которых основан на реакции присоединения водорода, во многих отношениях аналогичны широко распространенным никелевым аккумуляторам, однако, обладают, в отличие от последних, способностью запасать примерно в пять раз больше удельное количество водорода. Кроме того, такие батареи характеризуются более высокой эффективностью, малым весом, а также экологической и санитарной безопасностью по сравнению с наиболее продвинутыми в отношении этих качеств аккумуляторами на основе лития. Такие аккумуляторы могут найти широкое применение для питания персональных компьютеров и слуховых аппаратов.
Растворы фуллеренов в неполярных растворителях (сероуглерод, толуол, бензол, тетрахлорметан, декан, гексан, пентан) характеризуются нелинейными оптическими свойствами, что проявляется, в частности, в резком снижении прозрачности раствора при определенных условиях. Это открывает возможность использования фуллеренов в качестве основы оптических затворов- ограничителей интенсивности лазерного излучения..
Возникает перспектива использования фуллеренов в качестве основы для создания запоминающей среды со сверхвысокой плотностью информации. Фуллерены могут найти применение в качестве присадок для ракетных топлив, смазочного материала.
Большое внимание уделяется проблеме использования фуллеренов в медицине и фармакологии. Обсуждается идея создания противораковых медицинских препаратов на основе водо-растворимых эндоэдральных соединенийфуллеренов с радиоактивными изотопами. (Эндоэдральные соединения – это молекулы фуллеренов, внутри которых помещен один или более атомов какого- либо элемента). Найдены условия синтеза противовирусных и противораковых препаратов на основе фуллеренов. Одна из трудностей при решении этих проблем – создания водорастворимых нетоксичных соединений фуллеренов, которые могли бы вводиться в организм человека и доставляться кровью в орган, подлежащий терапевтическому воздействию.
Применение фуллеренов сдерживается их высокой стоимостью, которая складывается из трудоемкости получения фуллереновой смеси и из выделения из нее отдельных компонентов.
1.6.Углеродные нанотрубки
Структура нанотрубок
Наряду со сфероидальными углеродными структурами, могут образовываться также и протяженные цилиндрические структуры, так называемые нанотрубки, которые отличаются широким разнообразием физико-химических свойств.
Идеальная нанотрубка представляет собой свернутую в цилиндр графитовую плоскость, т.е. поверхность, выложенную правильными шестиугольниками, в вершинах которых расположены атомы углерода..).
Параметр, указывающим координаты шестиугольника, который в результате сворачивания плоскости должен совпасть с шестиугольником, находящимся в начале координат, называется хиральностью нанотрубки и обозначается набором символов (т, п). Хиральностьнанотрубки определяет ее электрические характеристики.
Как показали наблюдения, выполненные с помощью электронных микроскопов, большинство нанотрубок состоят из нескольких графитовых слоев, либо вложенных один в другой, либо навитых на общую ось.
Однослойные нанотрубки
На рис. 4 представлена идеализированная модель однослойной нанотрубки. Такая трубка заканчивается полусферическими вершинами, содержащими наряду
с правильными шестиугольниками, также по шесть правильных пятиугольников. Наличие пятиугольников на концах трубок позволяет рассматривать их как предельный случай молекул фуллеренов, длина продольной оси которых значительно превышает их диаметр.
Структура однослойных нанотрубок, наблюдаемых экспериментально, во многих отношениях отличается от представленной выше идеализированной картины. Прежде всего, это касается вершин нанотрубки, форма которых, как следует из наблюдений, далека от идеальной полусферы.
Многослойные нанотрубки
Многослойные нанотрубки отличаются от однослойных значительно более широким разнообразием форм и конфигураций как в продольном, так и в поперечном направлении. Возможные разновидности поперечной структуры многослойных нанотрубок представлены на рис. 5. Структура типа "русской матрешки" (russian dolls) представляет собой совокупность коаксиально вложенных друг в друга однослойных нанотрубок (рис 5 а). Другая разновидность этой структуры, показанная на рис. 5 б, представляет собой совокупность вложенных друг в друга коаксиальных призм. Наконец, последняя из приведённых структур (рис. 5 в), напоминает свиток. Для всех приведённых структур расстояния между соседними графитовыми слоями близко к величине 0,34 нм, т.е. расстоянию между соседними плоскостями кристаллического графита. Реализация той или иной структуры в конкретной экспериментальной ситуации зависит от условий синтеза нанотрубок.
Следует иметь в виду, что идеализированная поперечная структура нанотрубок, в которой расстояние между соседними слоями близко к значению 0,34 нм и не зависит от аксиальной координаты, на практике искажается вследствие возмущающего воздействия соседних нанотрубок.
Наличие дефектов приводит также к искажению прямолинейной формы нанотрубки и придаёт ей форму гармошки.
Другой тип дефектов, нередко отмечаемых на графитовой поверхности многослойных нанотрубок, связан с внедрением в поверхность, состоящую преимущественно из правильных шестиугольников, некоторого количества пятиугольников или семиугольников. Это приводит к нарушению цилиндрической формы, причём внедрение пятиугольника вызывает выпуклый изгиб, в то время как внедрение семиугольника способствует появлению вогнутого изгиба. Таким образом, подобные дефекты вызывают появление изогнутых и спиралевидных нанотрубок.
Структура наночастиц
В процессе образования фуллеренов из графита образуются также наночастицы. Это замкнутые структуры, подобные фуллеренам, но значительно превышающие их по размеру. В отличие от фуллеренов, они также как и нанотрубки могут содержать несколько слоев., имеют структуру замкнутых, вложенных друг в друга графитовых оболочек.
В наночастицах, аналогично графиту, атомы внутри оболочки связаны химическими связями, а между атомами соседних оболочек действует слабое ван-дер-ваальсово взаимодействие. Обычно оболочки наночастиц имеют форму близкую к многограннику. В структуре каждой такой оболочки, кроме шестиугольников, как в структуре графита, есть 12 пятиугольников, наблюдаются дополнительные пары из пяти и семиугольников. Электронно-микроскопическое изучение формы и строения углеродных частиц в фуллерено-содержащем конденсате было недавно проведено в работах Jarkovа S.M., Кашкина В.Б.
Получение углеродных нанотрубок
Углеродных нанотрубок образуются при термическом распыление графитового электрода в плазме дугового разряда, горящей в атмосфере гелия. Этот метод, как и метод лазерного распыления, лежащий в основе эффективной технологии получения фуллеренов, позволяет получать нанотрубки в количестве, достаточном для детального исследования их физико-химических свойств.
Нанотрубка может быть получена из протяжённых фрагментов графита, которые далее скручиваются в трубку. Для образования протяжённых фрагментов необходимы специальные условия нагрева графита. Оптимальные условия получения нанотрубок реализуются в дуговом разряде при использовании электролизного графита в качестве электродов.
Среди различны продуктов термического распыления графита (фуллерены, наночастицы, частицы сажи) небольшая часть (несколько процентов) приходится и на многослойные нанотрубки, которые частично прикрепляются к холодным поверхностям установки, частично осаждаются на поверхности вместе с сажей.
Однослойные нанотрубки образуются при добавлении в анод небольшой примеси Fe, Co, Ni, Cd (т. е. добавлением катализаторов). Кроме того, однослойные нанотрубки получаются при окислении многослойных нанотрубок. С целью окисления многослойные нанотрубоки обрабатываются кислородом при умеренном нагреве, либо кипящей азотной кислотой, причём в последнем случае происходит удаление пятичленных графитовых колец, приводящее к открытию концов трубок Окисление позволяет снять верхние слои с многослойной трубки и открыть её концы. Так как реакционная способность наночастиц выше, чем у нанотрубок, то при значительном разрушении углеродного продукта в результате окисления доля нанотрубок в оставшейся её части увеличивается.
При электродуговом способе получения фуллеренов часть материала, разрушающегося под действием дуги графитового анода, осаждается на катоде. К окончанию процесса разрушения графитового стержня данное образование вырастает настолько, что охватывает собой всю область дуги. Этот нарост имеет форму чаши, в объем которого введен анод. Физические характеристики катодного нароста сильно отличаются от характеристик графита, их которого состоит анод. Микротвердость нароста 5.95 ГПа (графита –0.22 ГПа), плотность нароста 1.32 г/см 3 (графит -2.3 г/см 3), удельное электрическое сопротивление нароста составляет 1.4*10 -4 Ом м, что практически на порядок больше, чем у графита (1.5*10 -5 Ом м). При 35 К обнаружена аномально высокая магнитная восприимчивость нароста на катоде, что позволило предположить, что нарост состоит, в основном, из нанотрубок (Белов Н.Н.).
Свойства нанотрубок
Широкие перспективы использования нанотрубок в материаловедении открываются при капсулипровании внутрь углеродных нанотрубок сверхпроводящих кристаллов (например, ТаС). В литературе описана следующая технология. Использовался дуговой разряд постоянного тока ~30 А при напряжении 30 В в атмосфере гелия с электродами, представляющими собой спрессованную смесь таллиевой пудры с графитовым пигментом. Межэлектродное расстояние составляло 2-3 мм. С помощью туннельного электронного микроскопа в продуктах термического разложения материала электродов было обнаружено значительное количество кристаллов ТаС, капсулированных в нанотрубки . х арактерный поперечный размер кристаллитов составлял около 7 нм, типичная длина нанотрубок – более 200 нм. Нанотрубки представляли собой многослойные цилиндры с расстоянием между слоями 0,3481 ±0,0009 нм, близким к соответствующему параметру для графита. Измерение температурной зависимости магнитной восприимчивости образцов показали, что капсулированные нанокристаллы, переходят в сверхпроводящее состояние при Т=10 К.
Возможность получения сверхпроводящих кристаллов, капсулированных в нанотрубки, позволяет изолировать их от вредного воздействия внешней среды,например, от окисления, открывая тем самым путь к более эффективному развитию соответствующих нанотехнологий..
Большая отрицательная магнитная восприимчивость нанотрубок указывает на их диамагнитные свойства. Предполагают, что диамагнетизм нанотрубок обусловлен протеканием электронных токов по их окружности. Величина магнитной восприимчивости не зависит от ориентации образца, что связано с его неупорядоченной структурой. Относительно большое значение магнитной восприимчивости указывает на то, что, по крайней мере, в одном из направлений эта величина сравнима с соответствующим значением для графита. Отличие температурной зависимости магнитной восприимчивости нанотрубок от соответствующих данных для других форм углерода указывает на то, что углеродные нанотрубки являются отдельной самостоятельной формой углерода, свойства которой принципиально отличаются от свойств углерода в других состояниях .
Применение нанотрубок
В основе многих технологических применений нанотрубок лежит такое их свойство, как высокая удельная поверхность (в случае однослойной нанотрубки около 600 кв. м. на 1/г), что открывает возможность их использования в качестве пористого материала в фильтрах и т.д.
Материал нанотрубок с успехом может использоваться в качестве несущей подложки для осуществления гетерогенного катализа, причем каталитическая активностьоткрытых нанотрубок заметно превышает соответствующий параметр длязамкнутыхнанотрубок.
Возможно использование нанотрубок с высокой удельной поверхность в качестве электродов для электролитических конденсаторов с большой удельной мощностью.
Углеродные нанотрубки хорошо себя зарекомендовали в экспериментах по использованию их в качестве покрытия, способствующего образованию алмазной пленки. Как показывают фотографии, выполненные с помощью электронного микроскопа, алмазная пленка, напыленная на пленку нанотрубок, отличается в лучшую сторону в отношении плотности и однородности зародышей от пленки, напыленной на С 60 и С 70 .
Такие свойства нанотрубки, как ее малые размеры, меняющаяся в значительных пределах в зависимости от условий синтеза, электропроводность, механическая прочность и химическая стабильность, позволяют рассматривать нанотрубку в качестве основы будущих элементов микроэлектроники. Расчетным путем доказано, что введение в идеальную структуру нанотрубки в качестве дефекта пары пятиугольник–семиугольник изменяет ее электронные свойства. Нанотрубка с внедренным в нее дефектом может рассматриваться как гетеропереход металл-полупроводник, который, в принципе, может составить основу полупроводникового элемента рекордно малых размеров.
Нанотрубки могут служить основой тончайшего измерительного инструмента, используемого для контроля неоднородностей поверхности электронных схем.
Интересные применения могут получить нанострубки при заполнении их различными материалами. При этом нанотрубка может использоваться как в качестве носителя заполняющего ее материала, так и в качестве изолирующей оболочки, предохраняющей данный материал от электрического контакта, либо от химического взаимодействия с окружающими объектами.
ЗАКЛЮЧЕНИЕ
Хотя фуллерены имеют короткую историю, это направление науки быстро развивается, привлекая к себе все новых исследователей. Эта область науки включает три направления: физика фуллеренов, химия фуллеренов и технология фуллеренов.
Физика фуллеренов занимается исследованием структурных, механических, электрических, магнитных, оптических свойств фуллеренов и их соединений в различных фазовых состояниях. Сюда относится также изучение характера взаимодействия между атомами углерода в этих соединениях, спектроскопия молекул фуллеренов, свойства и структура систем, состоящих из молекул фуллеренов. Физика фуллеренов является наиболее продвинутой ветвью в области фуллеренов.
Химия фуллеренов связана с созданием и изучением новых химических соединений, основу которых составляют замкнутые молекулы углерода, а также изучает химические процессы, в которых они участвуют. Следует отметить, что по концепциям и методам исследования это направление химии во многом принципиально отличается от традиционной химии.
Технология фуллеренов включает в себя как методы производства фуллеренов, так и различные их приложения.
СПИСОК ЛИТЕРАТУРЫ
1. Соколов В. И., Станкевич И. В. Фуллерены-новые аллотропные формы углерода: структура, электронное строение и химические свойства//Успехи химии, т.62 (5), с.455, 1993.
2. Новые направления в исследованиях фуллеренов//УФН, т. 164 (9), с. 1007, 1994.
3. Елецкий А. В., Смирнов Б.М. Фуллерены и структуры углерода//УФН, т. 165 (9), с.977, 1995.
4. Золотухин И.В. Фуллерит – новая форма углерода//СОЖ №2, с.51, 1996.
5. Мастеров В.Ф. Физические свойства фуллеренов//СОЖ №1, с.92, 1997.
6. Лозовик Ю.В., Попов А.М. Образование и рост углеродных наноструктур – фуллеренов, наночастиц, нанотрубок и конусов//УФН, т. 167 (7), с. 151, 1997/
7. Елецкий А.В. .Углеродные нанотрубки//УФН, т.167(9), с.945, 1997.
8. Смолли Р.Е. Открывая фуллерены//УФН, т.168 (3), с.323, 1998 .
9. Чурилов Г.Н. Обзор методов получения фуллеренов//Материалы 2 межрегиональной конференции с международным участием «Ультрадисперсные порошки, наноструктуры, материалы», Красноярск, КГТУ, 5-7 октября 1999 г,. с. 77-87.
10. Белов Н.Н. и др. Строение поверхности катодного нароста, образующегося при синтезе фуллеренов // Аэрозоли т.4f, N1, 1998 г. с.25-29
11. Jarkov S.M.,. Titarenko Ya .N., Churilov G.N. Elektron microscopy studies off FCC carbon particles// Carbon, v. 36, N 5-6, 1998, p. 595-597
12. Кашкин В.Б., Рублева Т.В., Кашкина Л.В., Мосин Р.А. Цифровая обработка электронно-микроскопических изображений углеродных частиц в фуллерено-содержащей саже // Материалы 2 межрегиональной конференции с международным участием «Ультрадисперсные порошки, наноструктуры, материалы», Красноярск, КГТУ, 5-7 октября 1999 г,. с. 91-92
Подробности
До сих пор существуют различные мнения о природе углеродных тел, стоящих как бы между органическими и неорганическими образованиями. По крайней мере, большинство исследователей считает, что различные формы углерода (кристаллические и переходные) представляют собой высокомолекулярные соединения - гомоцепные неорганические полимеры углерода.
Хорошо известны две кристаллические формы углерода, встречающиеся в природе, - алмаз и графит.
В настоящее время разработаны различные способы получения искусственных алмазов, в том числе и с новыми качествами, расширяющими диапазон их применения . Например, в электронике благодаря своей исключительной стабильности алмаз является перспективным электродным материалом для теоретической и прикладной электрохимии. В медицине разработаны ультрадисперсные алмазы детонационного синтеза как средство коррекции перекисного окисления белков при злокачественном росте (лимфосаркомы). Они используются при создании лекарственных препаратов пролонгированного действия. В химии алмаз предполагают использовать в качестве перспективного носителя для гетерогенных катализаторов, хроматографических сорбентов, присадок к топливам.
В результате исследования была открыта новая кристаллическая форма углерода, названная карбпиом, и кумулены - линейные полимеры углерода . Карбин способен существовать в виде длинных цепей с умеренной конформационной жесткостью. Кумулены, как правило, представляют собой олигомерные соединения . Искусственным путем был получен лонсдегшит, впоследствии обнаруженный в составе метеоритов. В конце двадцатого столетия открыты новые аллотропические модификации, такие, как фуллерены и углеродные нанотрубки.
В основном состоянии углерод имеет электронную конфигурацию Is 2s 2p , в том числе два валентных (2р) электрона . В большинстве случаев в химических реакциях углерод проявляет себя как четырехвалентный элемент, что связано с переходом электрона с 25-орбитали на 2/?-орбиталь по схеме:
Для четырехвалентного углерода известны три валентных состояния, соответствующие sp -, sp -, ^-гибридизации электронов атомов углерода. Этим валентным состояниям соответствуют кристаллические формы трех гибридных разновидностей атомов углерода - алмаз, графит и карбин.
Алмаз представляет собой пространственный полимер, состоящий из атомов углерода s/Лгибридизации с тетраэдрическим расположением валентных связей.
Графиту соответствует паркетный полимер, построенный из атомов углерода s/Лгибридизации, расположенных в одной плоскости.
В карбине, имеющем линейную полимерную цепочку пальминово-го (-С=С-)„ или кумуленового (=С=С=С=)„ типов реализуется 5р-гибридное состояние атомов углерода. Следует отметить, что в углероде простая бт-связь прочнее, чем 7г-компоненты кратных связей С=С или С=С, что отражается на свойствах аллотропных форм углерода. Известно также большое число так называемых переходных форм углерода, аморфных и частично-кристаллических.
Изучение структуры и свойств переходных форм углерода было проведено В.И. Касаточкиным . Согласно развитой им концепции большое многообразие переходных форм углерода обусловлено сочетанием атомов углерода различного гибридного состояния. К ним относятся всевозможные коксы, продукты термического превращения полимеров, стеклоуглерод, углеродные волокна.
Термодинамически углерод наиболее устойчив в кристаллическом состоянии. Переходная форма предполагает возможность превращения углерода. Однако из-за высоких кинетических барьеров углерод в состоянии переходных форм необычайно стабилен и в обычных условиях может существовать бесконечно длительное время. Лишь под воздействием высоких температур происходят структурные превращения углерода.
На рис. 1.1 представлена схема строения углеродных веществ - не-графитирующегося углерода (а) и искусственного графита (б).

Рис. 1.1. Схема строения углеродных веществ: а - неграфитируюшийся углерод; 6 - искусственный графит
Углерод переходных форм обладает разнообразными ценными фи-зико-химическими и механическими свойствами и имеет большое практическое значение. Широкий диапазон изменения свойств углерода связан с особенностями его структуры. Известны три основных элемента его структуры, а именно турбостратная структура, аморфный углерод и надатомные образования высшего порядка.
Турбостратной называется слоистая структура углерода, в которой в отличие от структуры графита отсутствует закономерная ориентация слоев относительно гексагональной оси. Основой турбостратной структуры являются базисные плоскости, строение которых аналогично графитовым плоскостям. Они состоят из шестизвенных ароматических циклов (гексагонов) атомов углерода с тем же межатомным расстоянием (1,415 А), что и в плоскостях графита. Определенное число плоскостей, соединяясь между собой, образует пакеты. В отличие от идеального графита в пакетах турбостратной структуры плоскости расположены под разными углами относительно друг друга. Схема строения углерода с турбостратной структурой изображена на рис. 1.2.
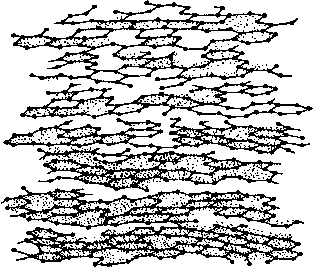
Рис. 1.2. Схема строения двумерноупорядоченного углерода с турбостратной структурой
В строго кристаллографическом понимании пакеты по структуре нельзя отнести к кристаллам, так как в них отсутствует трехмерная упорядоченность. В каждой плоскости пакета существует строгий порядок расположения атомов углерода, поэтому пакеты являются как бы двухмерными кристаллами, что позволяет в литературе турбостратную структуру углерода условно называть кристаллической.
Дальнейшее более полное развитие эти исследования получили в работах Р.Е. Франклина . В углероде переходных форм сосуществуют кристаллические турбостратные структуры и аморфный углерод. Количественное соотношение этих фракций трудно оценить. По данным , в коксе, полученном при термической деструкции поливинилиденхлорида, содержание аморфной фракции достигает 35%. Оно изменяется в зависимости от вида исходного сырья, используемого для получения углерода, условий его получения и конечной температуры обработки.
Схема строения неграфитирующегося углеродного вещества по Франклину представлена на рис. 1.1, а; на рисунке прямыми линиями обозначены базисные плоскости, а извилистыми - прослойки аморфного углерода между ними. В отличие от Франклина авторы работы для стеклоуглерода предлагают модель перепутанных лент, соединенных межмолекулярными связями с широким набором энергий. Прямые участки лент имеют размер около 100 А, соизмеримый со значением L
Определенным рентгеновским методом. Высота пакетов равна 40 А, что совпадает со значением L
Ленты неплотно упакованы, пронизаны порами, поэтому стеклоуглерод характеризуется низкой плотностью (1,45 г/см). В стеклоуглероде допускается наличие разветвленных лент.
Стеклоуглерод представляют и докембрийские шунгитовые породы, содержащие древнейший (2 млрд лет) некристаллический углерод .
Недостатком приведенных схем является то, что они не объясняют природу связей между лентами в направлении, перпендикулярном их плоскости. Большинство исследователей считают, что углерод находится только в тригональном состоянии, и плоскости между собой соединены не химическими, а слабыми межмолекулярными связями Ван-дер-Ваальса.
Можно представить иную надатомную организацию углерода , где турбостратные пакеты, а не отдельные слои могут быть теми структурными единицами, которые участвуют в построении структур высшего порядка. Пакеты связаны между собой различными гибридными формами аморфного углерода и образуют пространственный полимер. В процессе формирования ароматических сеток и их воссоединения в турбостратные пакеты на стадии карбонизации возникают пограничные.
дефекты, в том числе свободные валентности углерода, к которым присоединяются амор-фные цепи углерода, связывающие пакеты между собой. Схематически подобная структура углерода показана на рис. 1.3.
Аналогичная структурная схема была предложена В. И. Касаточкиным для витрена.
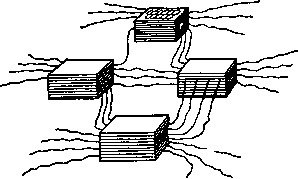
Рис. 1.3. Пространственная модель структур высшего порядка углерода
